鋳造では金属を扱う。金属は、錆びる。錆びるのは酸素と結合することだ。
それは酸化と呼ばれる。 製鉄は酸化鉄などから酸素を取り除いて鉄に戻すことだが、酸素で酸化された鉄を還元する作業だ。
酸化や還元とは、科学ではどう考えるのだろうか?
酸化と還元は電気化学の分野だ。鉄や銅を扱う鋳造技術者は、電気化学も学ぶ必要がある。
せっかく作った鉄鋳物が、発露により一夜で赤さびが出た経験を持つ者は多いはずだ。
最近は、電気自動車(EV)普及によって、電池が重要になってきた。電池も酸化還元を利用している。
それらをまとめて理解するのが、電気化学だという。
まず、電池のイメージ理解のため、現代の代表的な二次電池(充電・放電できるのを2次電池という)のLi電池の概念図を古川電機HPから紹介します。
電池の外では、
充電するときは電源から導電体を通って正極側に電流が流れ(電子は逆流)、
放電するときは正極から導電体の途中の外部負荷を通って負極へ電流が流れる(電子は逆流)。
電解質の中では、
Li+イオンが外部の電流を接続する回路を一周する電池内部の電流として移動する。
充電するときは、正極から負極へ+電気が流れる。正極で電子を失いLi+が発生し負極側へ移動、負極でLi+イオンが導電体を回ってきた電子を獲得してLiに還元される。
放電するときは、負極から正極に+電気が流れる。+イオンが負極で発生し正極へ移動。負極では元素が失った電子が導体で外側へ。正極では到着した+イオンが電子を得て還元される。
負極・正極では、それぞれー電子が受け渡しされ、LiとLi+が移り変わる。
同じLiが正極と負極に使われるのは、金属Liの電位に対してリチウム化合物の電位が約4V弱大きいことを利用。
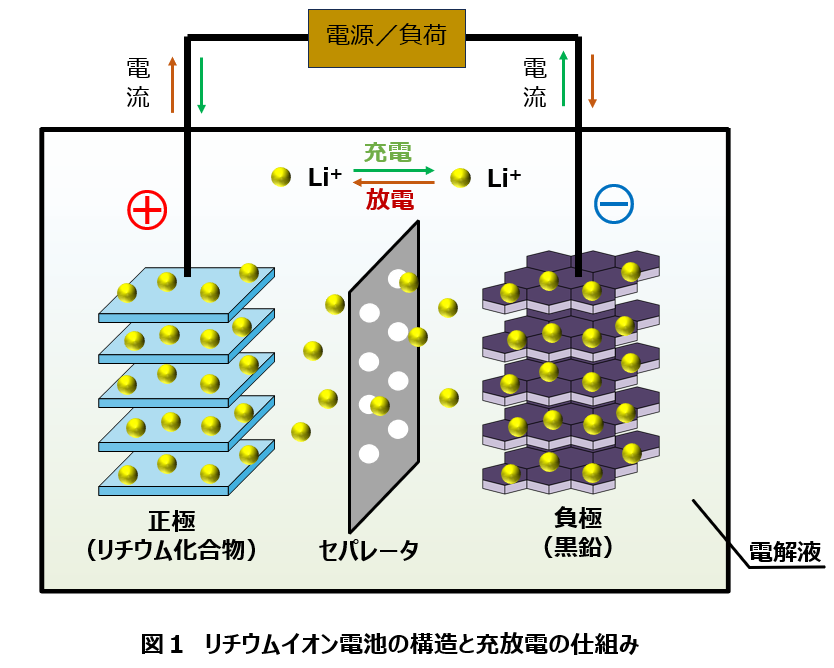
出典 古川電池 https://corp.furukawadenchi.co.jp/ja/news/news-20240717.html
電池の基礎理解なら、電気化学の教科書が一番
「電気化学の基礎」 京都大学大学院工学研究科 邑瀬邦明
http://www.echem.mtl.kyoto-u.ac.jp/documents/20150915r.pdf
酸化と還元
酸化=相手から電子を奪う 金属なら+イオンになり水に溶ける 酸素が水素から電子を奪って水分子に、鉄から電子を奪って酸化鉄に。
還元=相手に電子を与える 水中のーイオンが元素やガスに戻る(例: 塩酸の ClーイオンがCl2=塩素ガスに)
酸素と水素が反応して水ができる、2つの物質間の電子のやり取り
・酸素から見ると、水素の電子を奪って取り込み水分子に=相手(水素)を酸化
・水素から見ると、酸素に電子を与えて水分子に=相手(酸素)を還元
酸化力が強い=(相手からは)還元されやすい
還元力が強い=(相手からは)酸化されやすい
鉄が錆びる=鉄が酸素により酸化される=酸素が鉄で還元される
化学の世界では、誰かが「酸化」されたとき、必ずその裏側で誰かが「還元」されています。この関係を酸化還元反応と呼びます。
なぜ酸素が「還元」されたと言えるのか?
「酸化」と「還元」で、本質的なのは「電子(e-)の受け渡し」。
-
鉄(Fe)の視点:
鉄は酸素と結びつくとき、自分の持っている電子を酸素に投げ与えます。
電子を失う = 酸化 -
酸素(O)の視点:
酸素は鉄から投げられた電子を受け取ります。
電子を受け取る = 還元
つまり、鉄が錆びる(酸化鉄になる)プロセスにおいて、**「鉄は酸素によって酸化され、酸素は鉄によって還元された」**ということになります。
「電子を盗った・取られた」というのは、電子がどこか遠くへ飛んでいくわけではなく、**「原子と原子の間の、どこに電子が居座っているか」**という勢力図の変化を指しています。
1. 電子の「綱引き」:電気陰性度
原子にはそれぞれ、電子を自分の方へ引き寄せる強さ(電気陰性度)があります。
-
酸素: 電子が大好きで、引き寄せる力がめちゃくちゃ強い(綱引きの強豪)。
-
鉄: 電子を手放しやすく、引き寄せる力は弱め。
この二人が出会うと、真ん中にあった電子は一気に酸素側へ引き寄せられます。
2. 「所有権」が移動する
鉄と酸素が結びついて「酸化鉄」になるとき、電子は鉄の勢力圏から離れ、酸素の勢力圏へと移動します。
-
鉄から見れば: 自分の管理下から電子がいなくなった = 「盗られた(酸化)」
-
酸素から見れば: 自分の懐に電子が転がり込んできた = 「手に入れた(還元)」
「外には出ていない」というのは正解ですが、**「鉄という家から、酸素という隣の家へ引っ越した」**ような状態です。この「引っ越し」が起きた瞬間に、化学の世界では酸化・還元が成立したとみなします。
図は、ネットから引用 (Shtterstock)
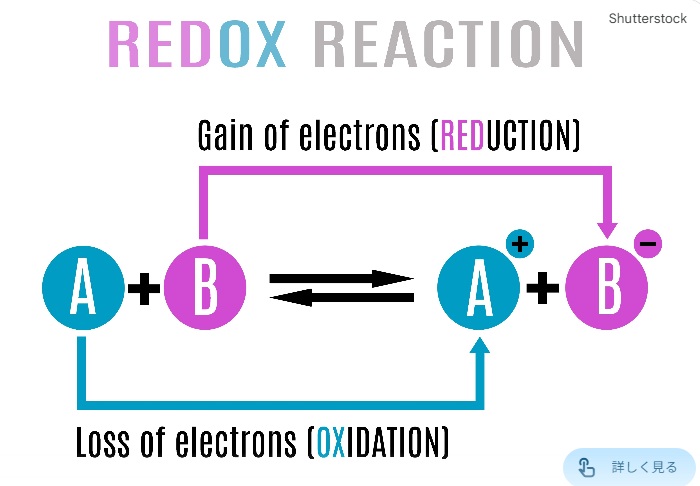
酸化剤と還元剤という考え方
この関係性を「相手をどうしたか」という役割で呼ぶこともあります。
-
鉄は「還元剤」: 自分は電子を盗られ=酸化されながら、相手(酸素)に電子を与え還元させる物質。
-
酸素は「酸化剤」: 自分は電子を獲得し=還元されながら、相手(鉄)に電子を与え酸化させる物質。
元素同士の酸化還元反応では、木が燃えると発熱するように、電子がより安定した状態になり差分のエネルギーが放出される。
一方、電極による酸化還元では、電子は導線を通じて移動する。この時、電極の外部からエネルギーを与えられたり与えたりして、外にエネルギーが減ったり発生したりする。
上記資料で、参照電解システムと測定法紹介
電気化学の考え方が、特徴的に出ている下図11で説明します。
HCL溶液に2対の電極を入れて、直流電圧を付加する。
右側が+で左側がーの電圧をかける。
電子はマイナスなので、+の電流とは逆方向に電線の中を流れ、電極間電位差により溶液の中では+イオンが右から左へ、マイナスイオンが逆方向に流れようとする。
右側の+電極では、マイナスイオンが+電極に引きつけられる。✙の電気が電極から液側に流れる=マイナスのイオンの電子がイオンから離れて電極へ流れる。
左側のー電極では、上記と反対の動きとなる。
溶液中では、HClが溶解してH+とClーに分離している。Clは強電解質で水中ではほぼ全量がイオンとして存在。
水素イオンは実際には水分子とくっついてH3O–として存在している。
右のCounter electrode表面では、溶液中のマイナス(-)の塩素イオンが電子を盗られ(=酸化)して塩素ガス発生。
塩素イオンは電子(e-)を余計に持つ。マイナスの電気を持つ塩素イオンはプラスの電極に引き付けられる。電位差=強い電場で電極がe-を取りあげる。塩素イオンは電子を盗られ(=酸化)塩素となり塩素ガスになる。
左のWorking electrode表面では溶液中のプラス(+)の水素イオンが電子をもらって(=還元)水素ガスが発生。
上記とは、電気的に逆になりマイナスの電極にプラスの水素イオンが引き寄せられる。欠乏していたマイナスの電子が電極から電位差で水素イオンに押し込まれて水素となる。
左の参照電極を標準の水素と電極の表面反応で基準値(電位0)としている。
参照電極とWorking electrodeとの電位差を電圧計で測定。
邑瀬「電気化学の基礎」より引用
電気化学において、標準電極電位(E)は、ある反応がどれだけ酸化されやすいか、あるいは還元されやすいかを示す重要な指標です。
一般的に、標準水素電極(SHE)を基準(0)とし、水溶液中における25°C、 1 atm、成分の活性度が 1 の状態での値を示します。
図の場合は、標準水素電極はHCl(塩酸)溶液でPH0の強酸性液。
中性(PH7)や強アルカリ(PH14)では値が変化する。
下図に示す電位表では、Hの標準電位はこの条件では0(基準値)ですが、強アルカリ(PH14)で、水分子とOH-の場合は ー0.83になります。
主要な標準電極電位一覧表(25°C)
電位が負に大きいほど還元力が強く(酸化されやすい)、正に大きいほど酸化力が強い(還元されやすい)ことを意味します。
表の中で、標準電位が低い(マイナス)の還元剤が負極になり、電位が比較して高い方が正極になります。
電池は、電位差が大きいことが必要で、絶対値より2つの物質間の電位差が利用されます。
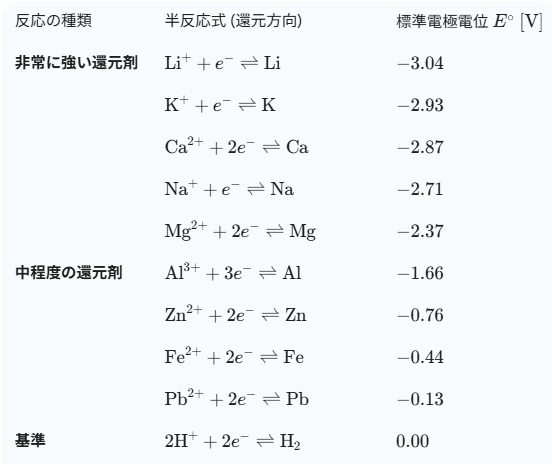
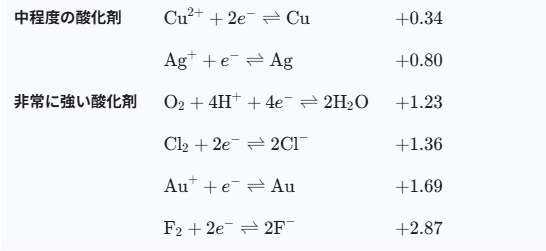
標準電極電位の意味
金Auは、+1.69Vです。酸素より酸化力が強いので酸素によっては酸化されない。
軌道電子が安定し追加の電子を必要とせず酸素から奪う理由もないので相互に電子のやり取り発生せず安定し反応しない。光の青を吸収するので補色の金色になる。
酸素は、外殻の軌道電子が2個不足し、電子を追加して補充したい(相手を酸化して電子を奪いたい)。
銀は、酸素より電位が低いので酸化されるけど表面に安定被膜を作ることや電位差が小さいので酸化が進みにくい。
フッ素Fは、+2.87と最強レベルの酸化力で、フッ素化合物が安定度が高い理由です。
上記のリストで、マイナスの還元と、プラスの酸化を組み合わせると電池ができます。
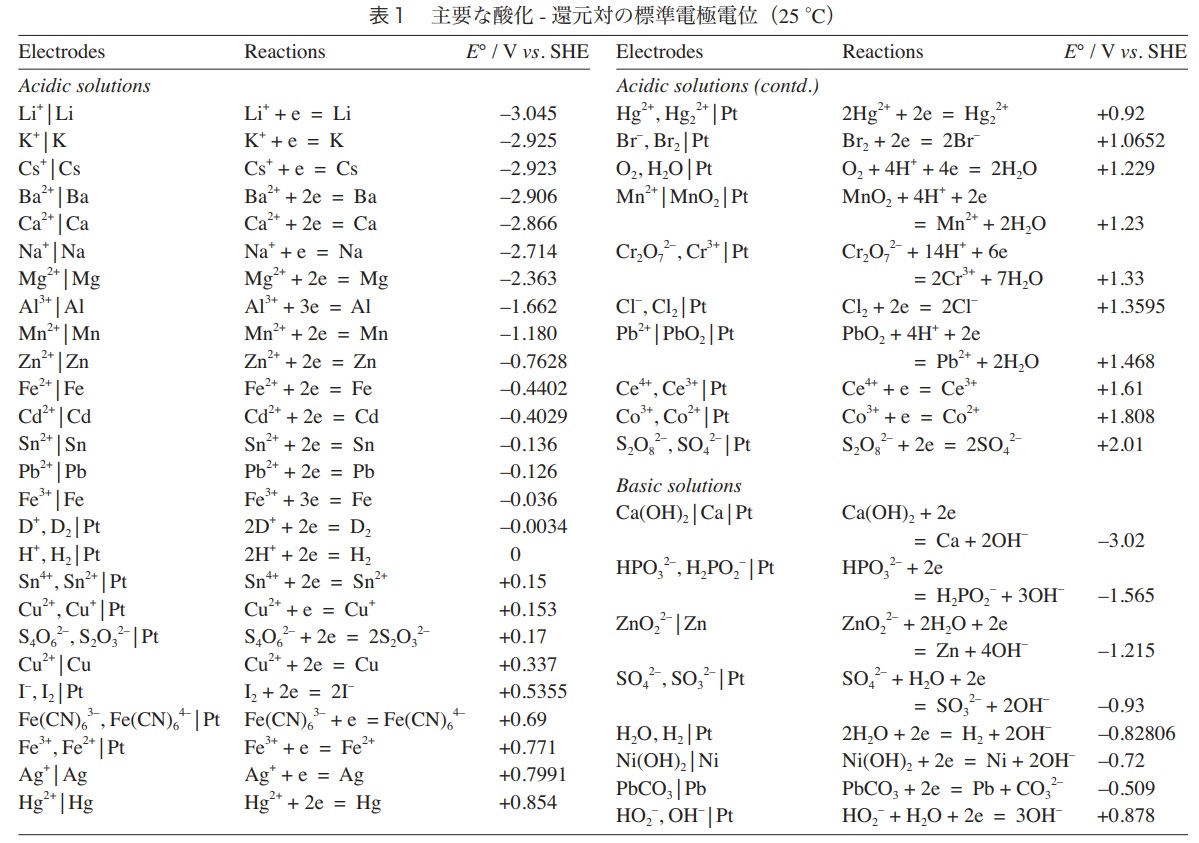
鉛(Pb)が電位低いのに電池として使えるのはなぜ?
AI(Gemini) の回答
鉛(Pb)の標準電極電位は−0.13Vで、一見すると「少しだけ卑な(還元されやすい)金属」という地味な立ち位置ですよね。
しかし、自動車のバッテリーなどで現役バリバリの「鉛蓄電池」として重宝されるのには、電位の数字だけでは見えない**「化学的なトリック」**がいくつか隠されています。
1. 相手役(正極)との「電位差」が非常に大きい
電池の電圧は、正極と負極の「電位の差」で決まります。鉛蓄電池の場合、負極だけでなく正極にも鉛の化合物を使いますが、その組み合わせが絶妙です。
-
負極(Pb): E∘−0.13 V
-
正極PbO2: E≈+1.69V
このペアにより、1セルあたり 約 2.0V という、水溶液系電池としてはかなり高い電圧を叩き出すことができます。
2. 生成物(PbSO4)が「溶けない」こと
これが最大のポイントです。普通の金属は反応するとイオンになって液に溶け出しますが、鉛蓄電池では硫酸(H2SO4)を電解液に使うため、反応の結果生じる「硫酸鉛(PbSO4)」が不溶性の結晶として電極の表面に留まります。
-
放電時: 鉛が溶け出さず、電極にくっついたまま。
-
充電時: 外部から電気を流すと、その場にある硫酸鉛が元の鉛(または酸化鉛)にスムーズに戻れる。
この「溶けずに待機している」性質のおかげで、何度も繰り返し充放電できる二次電池として成立しています。
3. 水の電気分解が起きにくい(水素過電圧)
理論上、電位が 0Vより低い金属を水溶液に入れると、水中の H+が還元されて水素ガスが発生し、電池が自己放電してしまいます。 しかし、鉛の表面では**「水素過電圧」**という現象が強く働き、水素ガスが発生する反応が非常に遅くなります。この「反応のサボり」のおかげで、マイナスの電位を持ちながらも水溶液中で安定して電気を蓄えておけるのです。
まとめると: 鉛は「単独で強い」のではなく、**「PbO2という強力な相方がいて」「硫酸の中で溶けずに踏ん張り」「水素発生を絶妙にいなしている」**からこそ、優秀な電池になれるのです。
鉛蓄電池の仕組みと特徴をわかりやすく解説
trendlineの説明が分かりやすい。ネットから引用紹介します。
鉛蓄電池がどのようにして電気を蓄え、放出するのかを理解するには、内部で起こる化学反応を知る必要があります。 ここでは、放電時と充電時それぞれの化学反応について、できるだけわかりやすく解説していきます。
放電時の化学反応
放電とは、蓄電池から電気エネルギーを取り出すプロセスのことです。 自動車のエンジンを始動させるときや、ライトを点灯させるときに起こる反応がこれにあたります。
鉛蓄電池の放電時には、負極の鉛(Pb)と正極の二酸化鉛(PbO2)がともに硫酸鉛(PbSO4)に変化します。 このとき、電解液中の硫酸(H2SO4)が消費され、水(H2O)が生成されます。
放電時の全体反応式は以下のとおりです。
Pb + PbO2 + 2H2SO4 → 2PbSO4 + 2H2O
この反応をもう少し詳しく見てみましょう。 負極では、鉛が硫酸イオンと反応して硫酸鉛になり、2個の電子を放出します。 この電子が外部回路を通って正極へと移動することで、電流が流れるのです。
|
電極 |
反応式 |
電子の動き |
|
負極(鉛) |
Pb + SO4²⁻ → PbSO4 + 2e⁻ |
電子を放出(酸化反応) |
|
正極(二酸化鉛) |
PbO2 + 4H⁺ + SO4²⁻ + 2e⁻ → PbSO4 + 2H2O |
電子を受け取る(還元反応) |
正極では、二酸化鉛が硫酸イオンと水素イオン、そして負極から流れてきた電子と反応します。 この結果、硫酸鉛と水が生成され、硫酸が減少します。
負極での酸化反応と正極での還元反応が同時に進行することで、電池全体として放電が行われるわけです。
放電が進むにつれて、電解液中の硫酸濃度は低下していきます。 これにより、電解液の比重(密度)も下がるため、比重計を使って電池の充電状態を確認することができます。 満充電時の比重は約1.28ですが、完全放電時には約1.10まで低下するのが一般的です。
- 放電時は両極とも硫酸鉛に変化する
- 電解液中の硫酸が消費されて水が生成される
- 電子は負極から外部回路を通って正極へ移動する
- 比重の低下で充電状態を推測できる
- 過放電は電池の寿命を縮める原因となる
充電時の化学反応
充電とは、外部から電気エネルギーを与えて、放電で変化した物質を元の状態に戻すプロセスです。 放電時の逆反応が進行することで、電池は再び電気を蓄えらた状態になります。
充電時の全体反応式は以下のようになります。
2PbSO4 + 2H2O → Pb + PbO2 + 2H2SO4
この反応は、放電時の反応式を逆向きにしたものです。 両極に付着していた硫酸鉛が分解され、負極では鉛(Pb)が再生し、正極では二酸化鉛(PbO2)が再生し硫酸が発生し液の硫酸濃度が濃くなる。
|
電極 |
反応式 |
電子の動き |
|
負極 |
PbSO4 + 2e⁻ → Pb + SO4²⁻ |
電子を受け取る(還元反応) |
|
正極 |
PbSO4 + 2H2O → PbO2 + 4H⁺ + SO4²⁻ + 2e⁻ |
電子を放出(酸化反応) |
充電時には、電解液中に硫酸が戻されるため、比重は再び上昇します。 充電の終期には比重が1.28程度まで回復し、これが満充電の目安となります。
ただし、充電の終盤には注意が必要です。 電池がほぼ満充電に近づくと、水の電気分解が起こりやすくなります。 このとき、正極側で酸素ガスが、負極側で水素ガスが発生します。
水の電気分解反応は以下のとおりです。
2H2O → 2H2 + O2
水素ガスは可燃性が高く、酸素と混合すると爆発の危険性があります。 そのため、充電中は十分な換気を行い、火気を近づけないことが重要です。 また、過充電を続けると電解液中の水分が減少し、電池の劣化が早まる原因にもなります。
最近の自動車やバッテリー充電器には、過充電を防止する制御機能が搭載されています。 これにより、充電が完了すると自動的に電流が制御され、ガスの発生を最小限に抑えることができます。
- 充電は放電の逆反応である
- 硫酸鉛が分解され、鉛と二酸化鉛と硫酸が再生される。
- 電解液の比重が上昇し、満充電で約1.28になる
- 充電終盤では水素と酸素のガスが発生する可能性がある
- 過充電防止機能付きの充電器の使用が推奨される
- 電解液の比重: 放電が進むと硫酸が減り、比重が下がる(目安:満充電1.28、放電終止1.10)。
- サルフェーション: 長期間放置や過放電により、負極に白い硫酸鉛の硬い結晶(サルフェーション)が付着し、充放電できなくなる。寿命は交流流して内部抵抗を測定するCCA(コールド・クランキング・アンペア)測定計器で、低温でも動作するかを判定。
- 電極の変化: 放電前は正極が褐色(PbO2)、負極が灰色(Pb)だが、放電後は両方とも白色(PBSO4)に変化する。


