ナトリウムイオン電池が次世代電池として有望だという。原理、開発現状、将来を調べた
電池の基礎理解勉強なら、電気化学の教科書が一番 推奨
「電気化学の基礎」 京都大学大学院工学研究科 邑瀬邦明
http://www.echem.mtl.kyoto-u.ac.jp/documents/20150915r.pdf
リチウムイオン電池は、正極にリチウム(元素記号:Li)をあらかじめ含ませた金属化合物、負極にはリチウムイオンの貯蔵ができる黒鉛を使用します。
リチウムイオン電池を大まかに説明すると、電池内の正極負極間を、リチウムイオンが行き来することで放電・充電を行う仕組みを持つ二次電池。
※黒鉛(グラファイト)は、「炭素原子が平らな網目状に結びつき、それが層のように積み重なったもの」。
相間の結合が弱く、柔らかく鉛筆の芯などにも使われる。
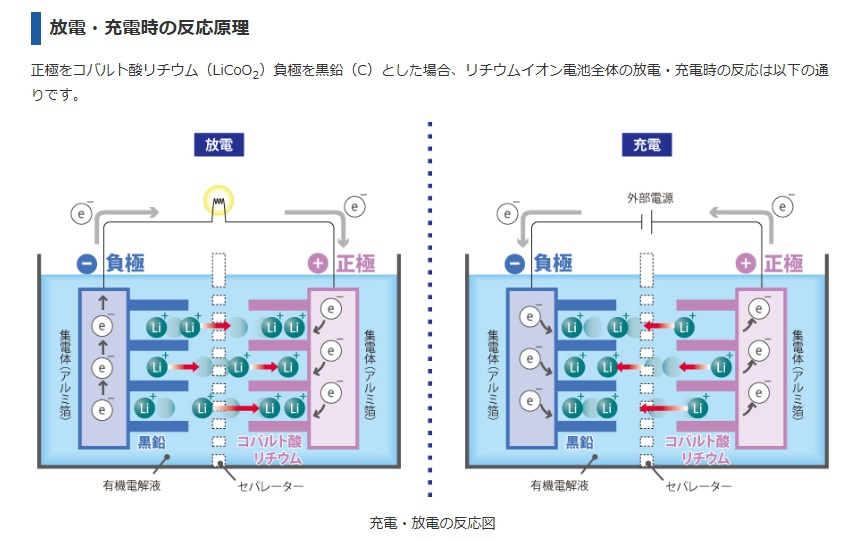
黒鉛の構造図(炭素原子が面を作り層間の結合は弱い)、ダイヤは立体結晶で硬い
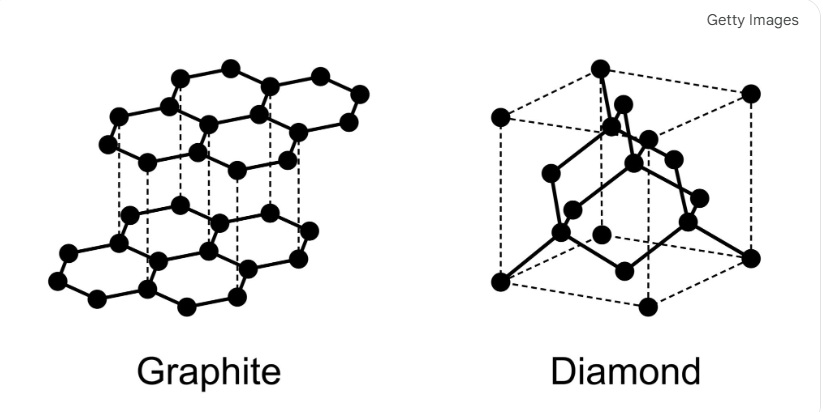
ナトリウムイオン電池原理図(中国の電池メーカー?の解説図)
AI(Gemini) の回答
ナトリウムイオン電池(NIB)は、現在主流のリチウムイオン電池(LIB)に代わる、あるいはそれを補完する次世代電池として、2026年現在、大きな転換点を迎えています。
特に「脱リチウム」によるコスト削減と、資源リスクの回避という文脈で、世界的に実用化が加速しています。
1. 原理:リチウムの「兄弟」のような仕組み
基本的な仕組みはリチウムイオン電池とほぼ同じ「ロッキングチェア型」です。
- 動作: 充電時にはナトリウムイオンが正極から負極へ移動し、放電時には負極から正極へ戻ります。この移動に伴って電子が流れ、電気が発生します。
- 材料の違い: リチウムの代わりに、食塩の主成分でもあるナトリウムをキャリア(運び手)として使います。
- 技術的課題だった点: ナトリウムイオンはリチウムイオンよりもサイズが大きく重いため、電極材料の隙間に出入りしにくく、電池の寿命や容量を確保するのが難しいとされてきました。しかし、近年の材料工学(特に「ハードカーボン」という負極材の進化)によってこれが克服されつつあります。
2. 開発の現状:2026年の立ち位置
2026年現在、ナトリウムイオン電池は「研究室」を飛び出し、「工場での量産」フェーズに入っています。
主な特徴とメリット
- 低コスト: ナトリウムは海水中などに無限に存在するため、リチウムに比べて原材料費を圧倒的に抑えられます。
- 低温に強い: -20°C以下の極寒環境でも性能が落ちにくく、冬場のEV走行距離減少という弱点をカバーできます。
- 安全性: 熱安定性が高く、発火リスクがリチウムイオン電池より低いとされています。また、電圧をゼロにして輸送できるため、物流面でも安全です。
- 急速充電: リチウムイオン電池よりも速く充電できる特性を持っています。
プレイヤーの動向
中国のCATLやBYDといった大手メーカーが、すでに第2世代のナトリウムイオン電池の量産を開始しており、航続距離300〜500km程度の小型電気自動車(EV)や、家庭・産業用の蓄電システムへの搭載が始まっています。
3. これからの予想:リチウムとの「棲み分け」
今後、すべての電池がナトリウムに置き換わるわけではなく、用途に応じた使い分けが進むと予想されます。
| 用途 | 推奨される電池 | 理由 |
|---|---|---|
| 高性能EV・スマホ | リチウムイオン | 軽さとエネルギー密度(長持ち)が最優先。 |
| 小型EV・低価格車 | ナトリウムイオン | 車体価格を抑えることが最優先。 |
| 定置型蓄電所 | ナトリウムイオン | 重さは関係なく、安さと寿命・安全性が重要。 |
| 寒冷地向け機器 | ナトリウムイオン | 冬場でも安定して動作するため。 |
今後のロードマップ予想
- 2026〜2028年: 鉛蓄電池(自動車の始動用バッテリーなど)のリプレイスが進み、低価格EV市場でのシェアが急拡大。
- 2030年以降: エネルギー密度がさらに向上し、中距離EVやドローンなど、より広い分野でリチウムイオン電池の強力なライバルへ。
- サプライチェーンの変革: リチウム資源を特定国に依存するリスクが減り、より持続可能なエネルギー社会へ移行。
「より安く、より安全に」というニーズに対し、ナトリウムイオン電池は非常に現実的な解となりつつあります。


